马蹄踏春启新程,科研逐光赴新篇
做ELISA实验的你,是否常有这样的困惑:同样的操作流程,为何有时数据精准、重复性拉满,有时却出现假阳性、信号微弱、曲线畸形?
其实,ELISA实验的成败,藏在每一个关键组分里。包被抗体/抗原、检测抗体、底物、洗涤液等,看似是简单的实验耗材,实则各自肩负“重任”,它们的作用机制直接决定了检测的特异性、灵敏度,甚至实验的最终走向。今天就和大家深度拆解ELISA关键组分的作用机制(以双抗体夹心法为例),读懂它们的“分工”,才能从根源上规避实验误差,让每一组数据都经得起推敲,科研之路一马当先!
核心组分①:包被抗体——ELISA的“基石”,筑牢检测根基
包被抗体是ELISA实验的“第一道防线”,也是整个检测体系的核心基石,相当于为目标分子搭建了一个“专属捕获平台”。
作用机制:将包被抗体固定在酶标板的微孔里,利用抗原与抗体的特异性结合,让后续加入的样本中目标分子能精准“锚定”在微孔内,避免被洗涤步骤冲走,为后续信号放大和检测打下基础。
关键影响:包被浓度、纯度、活性,直接决定了捕获目标分子的效率。包被浓度过高易导致非特异性结合(高背景),浓度过低则捕获不足(低信号);而包被物的活性不足,会直接导致结合能力下降,实验数据重复性差。
核心组分②:生物素化抗体-酶标亲和素——ELISA的“信号放大天团”,让微弱信号翻倍
如果说包被抗体是“捕获手”,那么生物素化抗体-酶标亲和素,就是协同作用的“信号放大天团”,二者配合能将抗原-抗体结合信号实现指数级放大,转化为可检测、可量化的视觉/仪器信号,尤其适合低丰度目标分子的检测。
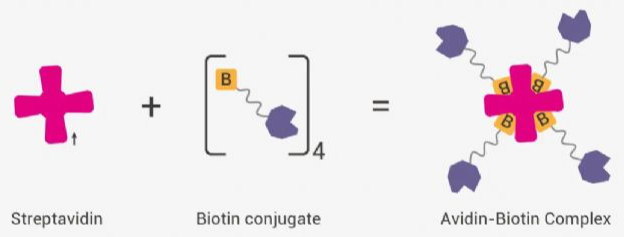
作用机制:生物素化抗体特异性结合已与包被物锚定的目标分子,形成“包被物-目标分子-生物素化抗体”的初级复合物,相当于为目标分子“标记”上专属识别位点;链霉亲和素作为核心“连接桥梁”,对生物素有极强的亲和力(亲和力是抗原抗体结合的1000倍以上),且一个链霉亲和素分子可同时结合4个生物素分子,搭建信号放大的“骨架”;HRP酶与亲和素共价结合,再特异性生物素化抗体,最终形成“包被物-目标分子-生物素抗体-酶标亲和素”的多级复合物。后续加入底物后,酶会催化底物发生显色反应,一个目标分子可带动多个酶分子,实现信号指数级放大。
关键影响:生物素抗体的特异性、标记效率、链霉亲和素的纯度等,直接决定了信号放大效果。标记效率过低或链霉亲和素纯度不够,则会导致信号放大不足、背景偏高,无法准确量化低丰度目标浓度。
核心组分③:底物——ELISA的“信号呈现者”,让数据可视化
生物素-亲和素系统放大了信号,底物则是将这种放大后的信号“呈现出来”的关键,它是连接酶促反应与数据读取的核心桥梁。
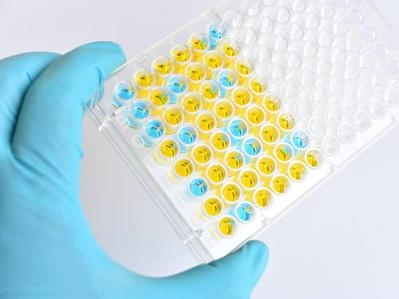
作用机制:HRP酶的特异性作用底物,在酶的催化下会发生显色反应——如TMB会从无色变为蓝色(终止后变为黄色),显色深度与目标分子的浓度正相关,后续通过酶标仪读取吸光度值,即可计算出目标分子的浓度。
关键影响:底物的纯度、稳定性、反应特异性等,会影响显色的清晰度与稳定性。纯度不足易出现背景显色,稳定性差则会导致反应失控,无法准确反映目标浓度。
核心组分④:洗涤液——ELISA的“清洁工”,扫清实验干扰
洗涤液看似简单,却是ELISA实验中“去杂留真”的关键,每一次洗涤,都是在为精准检测“扫清障碍”。
作用机制:洗涤液的核心作用是洗去酶标板微孔未结合的样本杂质、未结合的生物素化抗体,酶复合物等,只保留“包被物-目标分子-生物素抗体-酶标亲和素”的特异性复合物,避免未结合物质干扰实验结果。
关键影响:洗涤次数、时间直接影响实验背景与数据重复性。洗涤不彻底,会导致高背景;洗涤过度,可能会洗去特异性结合的复合物,导致信号微弱。
马年科研寄语
ELISA实验的每一组精准数据,都离不开核心组分的默契配合。读懂它们的作用机制,才能从根源上规避实验误差,少走弯路、高效出数。
瑞迪生物ELISA试剂盒均提供预包被酶标板,为客户省去包被的繁琐流程;采用高亲和力单克隆抗体;优化包被缓冲液,实现精准包被、稳定结合;搭配高纯度生物素、链霉亲和素,高效实现信号放大;配套底物,均经纯度检测与稳定性验证,特异性强、显色均匀;洗涤液缓冲体系稳定,可高效洗去未结合物质。
2026丙午马年,愿每一位科研人都能驭骏前行,深耕科研之路,让科研成果马到成功、源源不断!
