你有没有发现,身边女性似乎对疼痛更敏感、慢性疼痛的困扰也更多?临床中女性慢性疼痛的发病率远高于男性,背后不只是“耐受度”的差异,更是身体里的免疫细胞在悄悄发挥性别特异性作用!
2026年2月《Science Immunology》发表重磅研究,密歇根州立大学团队首次揪出了介导疼痛性别差异的“关键角色”——IL-10+单核细胞,从细胞和分子层面完整解释了“为什么男性疼痛缓解更快,女性更易陷入慢性疼痛”。
01.核心答案:一种免疫细胞,决定疼痛缓解的“男女速度差”
慢性疼痛是全球高发的健康问题,仅美国就有超1亿人受其困扰,而女性的患病风险是男性的数倍。此前大家普遍认为,这可能和激素、神经敏感度有关,但始终没有明确的核心机制。
本研究以皮肤炎症疼痛为模型,发现了雄性小鼠的疼痛在1周后就开始缓解,而雌性小鼠的疼痛感会持续更久,且二者的炎症程度并无差异——问题的核心在发炎部位的IL-10+单核细胞上。
科学家通过ELISA检测发现雄性小鼠发炎部位的IL-10蛋白水平显著高于雌性,对应的IL-10+单核细胞数量是雌性的2倍以上,这类细胞是身体里的“止痛小能手”,IL-10正是其分泌的关键止痛分子,在研究中人类临床数据也验证了这一点。研究者发现只要特异性减少这种免疫细胞,无论雌雄IL-10水平都大幅下降,疼痛缓解也会大幅延迟,这就证明它就是疼痛缓解的“核心执行者”。
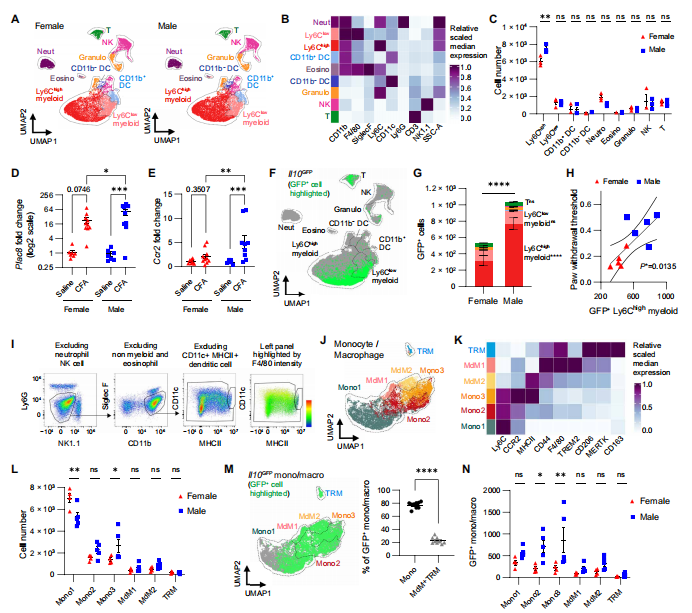
图1. 雄性小鼠体内 IL 10⁺单核细胞数量显著多于雌性小鼠。(A、B)CFA处理后皮肤免疫细胞的UMAP图及表面标志物相对表达热图,簇颜色与细胞类型对应。(C)CFA处理后皮肤免疫细胞数量。(D、E)WT小鼠CFA处理7天后皮肤中Plac8和Ccr2的mRNA水平。(F)UMAP图中浅绿色示皮肤免疫细胞群中的Il10-GFP细胞。(G)雌雄小鼠Il10-GFP⁺细胞数量。(H)CFA处理6天后,皮肤Il10-GFP⁺Ly6Chigh髓系细胞数量与机械痛阈值的相关性,R²=0.55,Pearson r=0.7444(雌性:红色三角;雄性:蓝色方块)。(I)单核细胞/巨噬细胞选择性圈门策略。(J)UMAP图展示3个单核细胞亚群、2个MdM亚群及1个TRM亚群。(K)热图示表面标志物相对表达,单核细胞亚群高表达Ly6C和CCR2。(L)各亚群在雌雄小鼠炎症皮肤中的分布。(M)左图UMAP浅绿色示Il10-GFP⁺单核细胞/巨噬细胞分布;右图为其单核细胞/巨噬细胞占比。(N)Il10-GFP⁺单核细胞/巨噬细胞定量。
02.工作原理:免疫细胞与神经的“直接对话”,精准止痛
很多人以为,免疫细胞只管“消炎”,间接帮着止痛。而这项研究推翻了这个认知,IL-10+单核细胞会直接和感觉神经“沟通”,精准抑制疼痛感。 这些免疫细胞分泌的IL-10分子,会找到外周感觉神经元表面的“接收器”(IL-10R1),结合后直接降低神经元的兴奋性,让疼痛信号无法顺利传导,从而实现快速止痛。实验还表明男女神经元的“接收器”数量也无差异,疼痛的性别差纯粹是因为免疫细胞分泌的“止痛分子”多少不同。
实验中,给发炎部位注射人工合成的IL-10,可检测到局部IL-10浓度升高,同时雌雄小鼠的疼痛缓解也加快;反之,阻断这种分子的作用,疼痛感就会迟迟不消,这也印证了它的核心止痛作用。
03.幕后调控:雄激素,竟是“止痛细胞”的“激活剂”
为什么男性的IL-10+单核细胞更多?研究找到了关键的上游调控因子——雄激素。 研究者给雌性小鼠补充雄激素后,发现其体内IL-10蛋白水平显著提升,对应的“止痛免疫细胞”数量大幅增加,疼痛缓解速度直接追上雄性;而抑制雄性小鼠的雄激素作用后,IL-10表达水平显著下降,免疫细胞减少,疼痛缓解也会变慢。 简单讲,雄激素会直接“激活”单核细胞,让它更高效地分泌止痛分子,这也是男性疼痛缓解更快的重要原因。
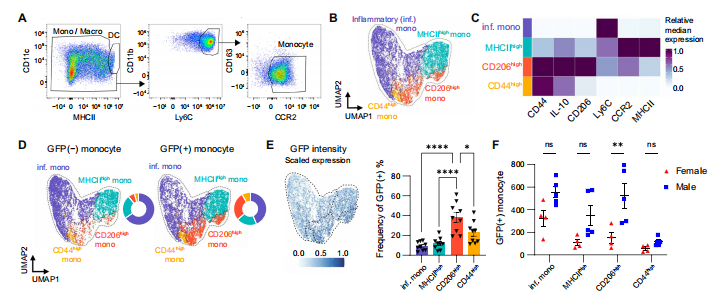
图2. 与雌性小鼠相比,雄性小鼠炎症皮肤中IL-10⁺ CD206high单核细胞更为普遍。(A)CFA处理后皮肤中,从其他CD45⁺细胞中鉴定单核细胞的流式细胞术圈门策略;MHCII/CD11c流式图与图2I一致。(B、C)CFA处理后皮肤单核细胞亚群的代表性UMAP图,由8只小鼠的20000个单核细胞随机筛选汇集生成;根据标志物表达,单核细胞被分为“炎症型”、MHCII型、CD206型和CD44型四个簇。(D)各簇在Il10-GFP⁺和Il10-GFP⁻单核细胞中的分布情况。(E)每个簇中Il10-GFP⁺单核细胞的频率。(F)每种性别各簇中Il10-GFP⁺单核细胞的定量统计。
04.惊喜发现:一种分子,能抹平疼痛的性别差异
研究还带来了一个极具应用价值的发现:促炎症消退脂质介质Resolvin D1(RvD1),能靶向提升雌雄小鼠体内的IL-10+单核细胞数量,并观察到IL-10水平均明显升高,有效消除了二者的疼痛缓解差异,让女性的疼痛缓解速度也能大幅提升。 这一发现为慢性疼痛的治疗提供了全新思路:未来或许可以通过靶向调控这种免疫细胞,开发出其它止痛干预手段,帮助更多慢性疼痛患者,尤其是女性患者摆脱困扰。 但研究表明,并非所有单核细胞都能止痛,CD206high亚型的单核细胞是分泌止痛分子的“主力军”,这也为后续的精准研究和干预,锁定了更具体的靶点。
这项研究也让我们看到男女在身体感受上的差异,很多时候并非“主观感受”,而是由细胞、分子层面的客观差异决定的,而这些隐藏的差异,正通过不断进步的生物检测技术被逐一揭开,让我们对自身的身体机制,有了更科学、更细致的认知。
原文链接 https://www.science.org/doi/10.1126/sciimmunol.adx0292
