巨噬细胞作为机体固有免疫的核心细胞,早已超越“吞噬细胞”的传统认知。近年来,越来越多的研究证实,其功能可塑性与异质性,在肿瘤、神经退行性疾病、代谢性疾病等重大疾病的发生、发展、转归中发挥着不可替代的调控作用,成为连接免疫与疾病的“桥梁”,也是近年来科研领域的核心研究靶点。作为深耕ELISA检测技术多年的厂家,现结合ELISA检测技术应用经验,梳理了巨噬细胞与三大疾病的核心关联,为相关研究提供实用参考。
巨噬细胞与肿瘤:肿瘤微环境的“关键调控者”
肿瘤相关巨噬细胞(TAM)是肿瘤微环境中数量最多的免疫细胞,其M1/M2极化状态直接决定肿瘤进展方向——M1型巨噬细胞具有促炎、抗肿瘤活性,可通过分泌TNF-α、IL-6等促炎因子抑制肿瘤生长;而M2型巨噬细胞则呈现抗炎、促肿瘤特性,通过分泌IL-10、TGF-β1、VEGF等因子,促进肿瘤血管生成、免疫逃逸及远处转移。
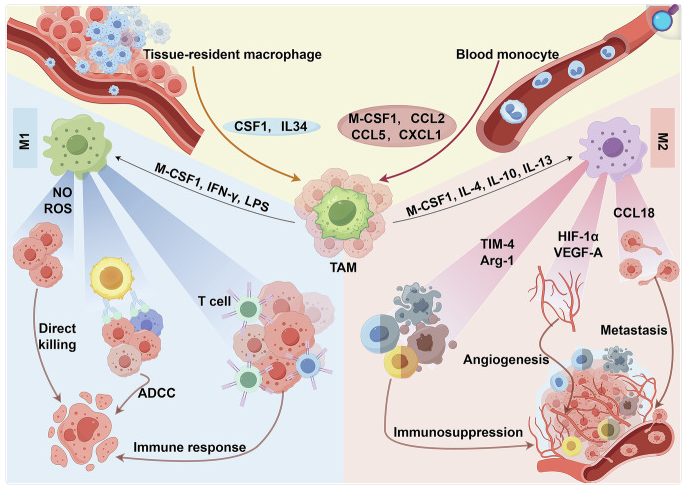
Distribution and density of tumor-associated macrophages in the tumor microenvironment.[Xu et al].
研究关键检测:核心关注TAM极化相关因子(TNF-α、IL-6、IL-10、TGF-β1、VEGF)的定量检测,ELISA技术因特异性强、操作便捷,成为该方向常规检测手段,需注意选择高灵敏度试剂盒,捕捉肿瘤微环境中低浓度因子表达变化。
巨噬细胞与神经退行性疾病:大脑“守护者”的功能失衡
小胶质细胞(中枢神经系统特化的巨噬细胞)是大脑的“免疫哨兵”,正常状态下可清除大脑内的Aβ斑块(阿尔茨海默病AD)、α-突触核蛋白(帕金森病PD)等异常蛋白,维持中枢神经系统稳态。当机体出现病理状态时,小胶质细胞被异常激活并向M1型极化,大量分泌TNF-α、IL-1β等促炎因子,引发慢性神经炎症,加剧神经元损伤,加速AD、PD等疾病的进展。
研究关键检测:重点检测小胶质细胞活化相关促炎因子(TNF-α、IL-1β、IL-6)及异常蛋白清除相关因子,因样本多为脑脊液、脑组织匀浆,ELISA检测需选择经样本基质优化的试剂盒,避免基质干扰,确保检测特异性。
巨噬细胞与代谢性疾病:代谢紊乱的“隐形推手”
在肥胖、非酒精性脂肪性肝炎(NASH)、糖尿病等代谢性疾病中,巨噬细胞的异常浸润与活化是核心致病因素之一。肥胖状态下,脂肪组织中巨噬细胞大量聚集并活化,分泌IL-6、TNF-α等促炎因子,引发脂肪组织慢性炎症,进而导致胰岛素抵抗;在NASH中,肝脏巨噬细胞(库普弗细胞)活化,促进肝纤维化进展。
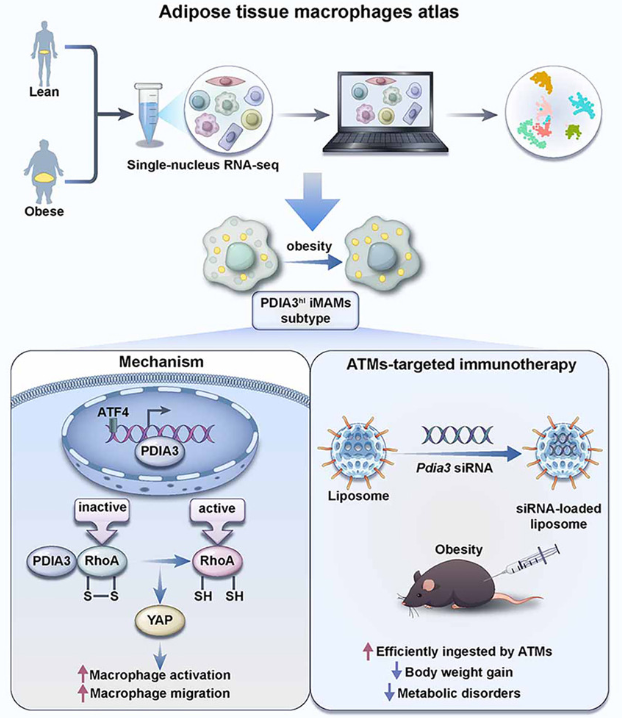
Distribution and density of tumor-associated macrophages in the tumor microenvironment.[Xu et al].
研究关键检测:核心检测脂肪组织、肝脏组织中巨噬细胞相关促炎因子(IL-6、TNF-α)及抗炎因子(IL-10),ELISA检测需适配脂肪组织匀浆、肝脏匀浆等样本。同时在ELISA 检测之前建议进行总蛋白定量,这是投稿阶段审稿人认可ELISA检测数据可靠性的重要一步。
共性:极化失衡是核心共性
尽管巨噬细胞在不同疾病中的具体作用机制存在差异,但核心共性均围绕“功能极化失衡”展开——M1/M2极化状态的异常转换,导致免疫平衡被打破,进而推动疾病进展。因此,精准检测巨噬细胞极化相关因子,明确其极化状态,是解析巨噬细胞在疾病中作用机制的关键,也是推动相关疾病诊断、治疗研究的核心基础。巨噬细胞与疾病的关联研究,正朝着精准化、多元化方向推进,从机制解析到靶向干预,每一步都离不开可靠的检测技术支撑。
参考文献:
Xu,J.S. et al. Dual roles and therapeutic targeting of tumor-associated macrophages in tumor microenvironments. Signal Transduction and Targeted Therapy, 2025, 10: 268.
Liu DH, et.al. Nucleotide metabolic rewiring enables NLRP3 inflammasome hyperactivation in obesity. Science, 2026, 391(6782):eadq9006. doi: 10.1126/science.adq9006. Epub 2026 Jan 15.
Luo,J.H.et.al. PDIA3 defines a novel subset of adipose macrophages to exacerbate the development of obesity and metabolic disorders. Cell Metabolism, 2024, 36(10): 2262-2280.E5.
Yang,X.M. et.al. Microglial polarization in Alzheimer's disease: Mechanisms, implications, and therapeutic opportunities. J Alzheimers Dis. 2025 Mar;104(1):3-13. doi: 10.1177/13872877241313223
Tardito,S. et.al. Macrophage M1/M2 polarization and rheumatoid arthritis: A systematic review. Autoimmunity Reviews,2019,18(11).
