长期以来,自身炎症领域几乎被 “IL-1β、IL-6、TNF-α”三大经典炎症因子主导,机制研究、靶点开发与临床诊疗大多围绕这类传统促炎因子展开。
聚焦于这三类因子的核心原因十分明确:它们诱导的炎症表型最直观、信号通路最清晰、临床验证最便捷。 IL-1β与TNF-α可直接引发高热、红肿、疼痛及急性期反应(CRP、血沉升高),且处于炎症小体下游,信号传导路径清晰易懂;加之IL-1抑制剂、TNF拮抗剂率先在临床取得疗效,进一步巩固了“自身炎症等同于传统炎症因子介导”的固有认知。
与之相对,以IFN-γ为核心的干扰素轴长期被忽略。干扰素虽同属炎症因子,但其作用模式更隐匿,主要由NK/CD8+T细胞分泌,不会直接引发典型急性高热,因此被归属于抗病毒免疫与自身免疫研究范畴,未被视作自身炎症的核心调控通路。
临床困境倒逼范式革新:传统治疗为何频频失效?
范式的突破往往由临床困境推动。以甲羟戊酸激酶缺乏症(MKD)为代表的经典自身炎症疾病,长期被归类为IL-1β驱动的炎症小体病,临床首选IL-1抑制剂治疗。但现实情况中大量患者对传统治疗反应不佳,重症病例更会快速进展为HLH/MAS样炎症危象,这表明:传统炎症因子可能并非此类疾病的核心驱动因素。
颠覆性发现:MKD真正元凶是IFN-γ风暴
近期发表于 Immunity 的一项研究打破了这一认知困局,并提出颠覆性结论:MKD的核心致病机制是NK细胞毒性缺陷引发的IFN-γ风暴。 MVK突变导致甲羟戊酸通路异常,造成蛋白异戊二烯化缺陷,进而导致NK细胞成熟障碍、细胞毒颗粒转运与极化异常,呈现出杀伤功能下降,却异常大量分泌IFN-γ的失衡表型;同时CD8+T细胞也存在相似功能缺陷,使机体无法有效清除病毒,持续免疫激活进一步放大IFN-γ释放,最终引发失控的全身性重症炎症。这一机制解释了传统IL-1靶向治疗无效的根本原因,也将干扰素轴推至自身炎症研究的核心位置。
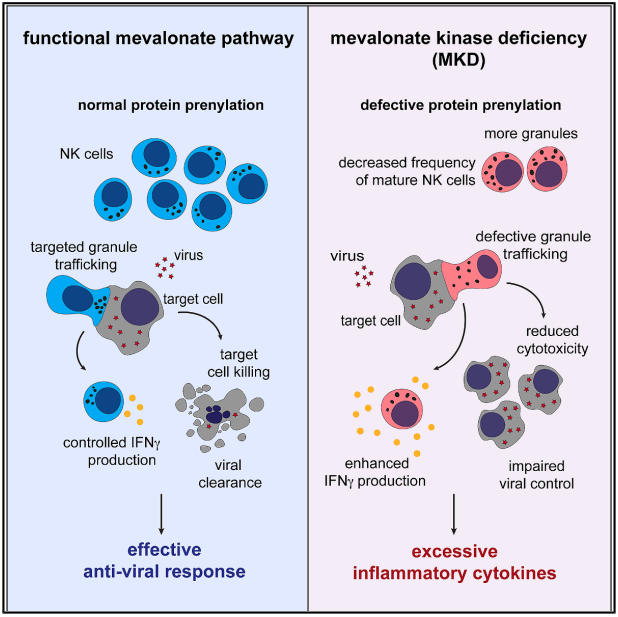
原文链接:https://www.cell.com/immunity/fulltext/S1074-7613(26)00138-X
干扰素轴为何能成为新赛道?
干扰素轴快速成为研究热点是因它拥有传统炎症因子无法比拟的普适性与临床转化价值:
1. 临床覆盖更广:IFN-γ信号异常参与不明原因发热、难治性炎症、感染/疫苗诱发发作、MAS/HLH等高危场景。
2. 机制层级更高:深度联动代谢-免疫交叉、细胞毒性免疫、JAK-STAT网络,是连接免疫缺陷与重症炎症的关键枢纽。
3. 转化路径清晰:JAK抑制剂可直接阻断下游信号,快速实现从机制到用药的闭环。
4. 创新空间巨大:避开IL-1β/NLRP3内卷,开辟课题方向。
转向新方向:干扰素轴开启全新研究格局
转向干扰素轴,研究者无需再局限于NLRP3、IL-1β等高度拥挤的成熟靶点,可聚焦NK/CD8+T细胞毒性、蛋白异戊二烯化、小G蛋白调控、干扰素下游趋化因子网络等方向。当传统炎症因子研究空间逐渐收窄,以IFN-γ为核心的干扰素轴,正以更上游的调控地位、更关键的重症驱动作用、更清晰的转化路径,成为自身炎症领域的下一个核心热点之一。
瑞迪生物相关指标:
|
货号 |
名称 |
上样量 |
|
RE1059H |
人γ干扰素(IFN-γ)酶联免疫吸附测定试剂盒 |
100μL |
|
RE1059HF |
MF-人γ干扰素(IFN-γ)酶联免疫吸附测定试剂盒 |
25μL |
|
RE1059M |
小鼠γ干扰素(IFN-γ)酶联免疫吸附测定试剂盒 |
100μL |
|
RE1059MF |
MF-小鼠γ干扰素(IFN-γ)酶联免疫吸附测定试剂盒 |
25μL |
|
RE3405M |
小鼠干扰素-γ受体1(IFN-γ R1)酶联免疫吸附测定试剂盒 |
100μL |
|
RE1059R |
大鼠γ干扰素(IFN-γ)酶联免疫吸附测定试剂盒 |
100μL |
|
RE1059RF |
MF-大鼠γ干扰素(IFN-γ)酶联免疫吸附测定试剂盒 |
25μL |
